可注射 “細胞積木”:科學家用 3D 顆粒復合材料構建功能性軟骨組織
發布時間:2025-08-21

膝關節損傷、骨關節炎等疾病正困擾著全球數以億計的人群。人體軟骨組織缺乏血管和神經,自我修復能力極弱,一旦受損往往難以自愈。目前,臨床常用的軟骨修復方法(如自體軟骨移植、人工關節置換等)存在供體來源有限、手術創傷大、植入物兼容性差等問題。 如何高效構建與天然軟骨結構、功能相似的替代組織,成為再生醫學領域的關鍵挑戰。
近日,《Advanced Materials》期刊發表的一項研究帶來了新突破。美國賓夕法尼亞大學和科羅拉多大學博爾德分校的科研團隊開發了一種可注射顆粒復合材料,將間充質基質細胞(MSC)形成的球狀體與透明質酸微凝膠顆粒混合,通過光照交聯技術穩定結構,成功構建出具有天然軟骨力學性能的工程化組織。
可注射性:微創手術的理想選擇
傳統組織工程支架往往需要通過手術植入,而這種復合材料在注射前呈流體狀態,可通過細針管直接注入軟骨缺損部位。研究顯示,當MSC球狀體與微凝膠以20:80或35:65的體積比混合時,材料表現出優異的剪切稀化特性——受外力時變稀便于注射,靜置后又能恢復結構,極大降低了手術創傷和操作難度。
細胞互作與組織融合:模擬天然發育過程
MSC球狀體本身含有高密度細胞,能自發形成細胞間連接(如N-鈣黏蛋白介導的相互作用),這對軟骨分化至關重要。而微凝膠顆粒作為不僅為細胞提供機械支撐,還通過孔隙結構允許營養物質擴散和細胞遷移。實驗表明,培養56天后,球狀體逐漸融合,分泌大量軟骨特異性細胞外基質(如Ⅱ型膠原、硫酸糖胺聚糖),形成連續的軟骨組織。
力學性能逼近天然軟骨
通過調控微凝膠的光交聯程度和顆粒比例,研究團隊實現了材料力學性能的精準調控。培養至56天時,35:65比例的復合材料抗壓強度達到580 kPa,接近天然透明軟骨的力學范圍(0.1-1.6 MPa)。更重要的是,其內部基質分布均勻,Ⅱ型膠原與Ⅰ型膠原的比例理想,提示形成了類似天然軟骨的透明質樣組織。
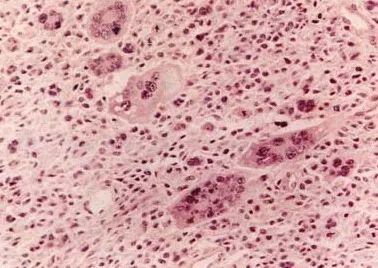
實驗驗證
①體外構建:顆粒比例決定 “搭建效率”
研究人員首先通過模擬計算(Cinema4D 軟件)分析了球狀體與微凝膠的混合比例對結構穩定性的影響。當微凝膠比例過低(如50:50)時,材料易坍塌;而比例過高(如20:80)時,微凝膠間的交聯網絡能有效維持結構。實驗證實,20:80和35:65比例的復合材料在培養過程中保持形態穩定,且35:65組因細胞密度更高,基質分泌量增加約50%。
②功能測試:基質分泌與力學性能雙達標
通過生化分析,培養56天的復合材料中,硫酸糖胺聚糖(sGAG)和膠原含量分別達到天然軟骨的80% 和70%以上。免疫組化染色顯示,基質中Ⅱ型膠原分布廣泛,而Ⅰ型膠原含量極低,表明形成了高質量的軟骨組織。此外,材料的孔隙率從初始20%逐漸被新生基質填充,進一步增強了力學性能。
③與天然組織的整合:向臨床轉化邁進
在體外軟骨環模型中,35:65比例的復合材料與天然軟骨的整合強度達到60 kPa,雖低于天然軟骨塊(170 kPa),但顯著高于單純微凝膠支架(20 kPa)。這意味著,新構建的軟骨組織能與周圍天然組織形成機械連接,為后續體內修復實驗奠定了基礎。
這項研究為軟骨組織工程提供了全新思路,但仍有優化空間。例如,微凝膠的降解速率與基質分泌的匹配度、材料與天然組織的整合強度提升等,都是后續研究的重點。研究團隊表示,下一步將在動物模型中驗證材料的體內修復效果,同時探索其在其他組織(如骨、肌肉)工程中的應用潛力。或許在不久的將來,通過微創注射實現組織再生的技術能讓軟骨損傷患者擺脫開刀之苦,這不僅是材料科學的進步,更是再生醫學向臨床轉化的重要一步。
參考文獻
Di Caprio N, et al. Adv Mater. 2024;36(14):e2312226.
注:本文僅供科普參考,具體治療方案請遵醫囑。

 0311-86576536
0311-86576536 新聞中心
新聞中心 風采展示
風采展示 信息公告
信息公告
 公眾號
公眾號 視頻號
視頻號

