儲存造血干細胞,點亮血友病治愈曙光
發(fā)布時間:2025-08-20

2025年世界血友病日的主題是“創(chuàng)新療法,改寫未來”。血友病,一種因凝血因子缺乏導致的遺傳性出血性疾病,患者自幼面臨關節(jié)反復出血、肌肉血腫甚至危及生命的風險。全球約40萬患者中,中國占14.4萬,但僅有30%接受規(guī)范治療。傳統(tǒng)凝血因子替代治療雖能緩解癥狀,卻無法根治,患者需終身用藥,經濟負擔沉重,且存在抗體產生和藥物可及性不足的困境。 在這一背景下,造血干細胞(HSC)及其衍生的基因治療技術,正以革命性姿態(tài)叩響治愈之門。
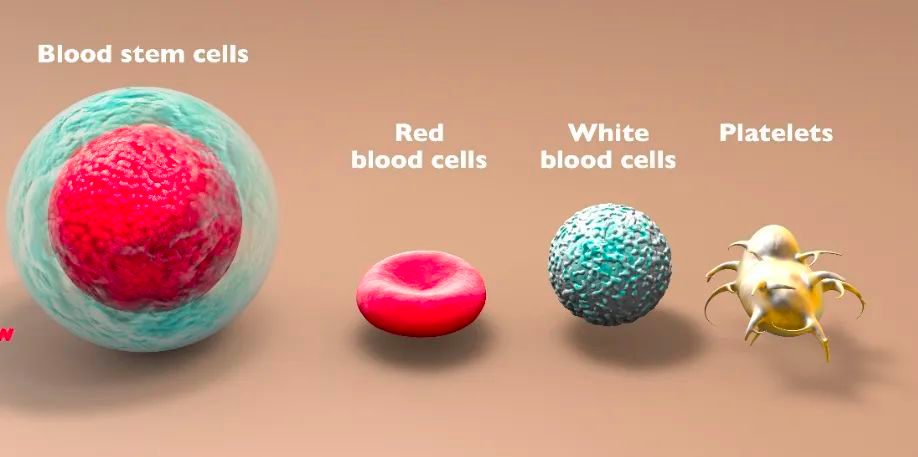
1.造血干細胞的生物學特性與治療潛力
造血干細胞具有自我更新和多向分化能力,是血液系統(tǒng)修復的核心“種子細胞”。通過移植或基因修飾,HSC可重建患者造血系統(tǒng),從根本上糾正凝血因子缺陷。例如,異基因HSC移植已成功治愈重型地中海貧血和再生障礙性貧血,為血友病治療提供借鑒。
2. 基因治療:HSC載體的突破性應用
近年來,基因治療成為血友病領域的焦點。通過腺相關病毒(AAV)或慢病毒載體,將正常凝血因子基因(FⅧ或FⅨ)導入患者HSC中,使其持續(xù)分泌功能蛋白。2022年,中國首項AAV載體血友病B基因治療臨床試驗取得里程碑進展,患者凝血因子活性顯著提升。目前,多款靶向肝臟的AAV基因療法已進入III期臨床,預計未來5年內有望獲批。
案例啟示:2024年,國內某基因治療項目中,一名重度血友病A患者接受基因修飾的HSC移植后,F(xiàn)Ⅷ活性穩(wěn)定在正常水平的15%-20%,無需再依賴外源性凝血因子輸注。
自體儲存:規(guī)避排異風險,實現(xiàn)個體化治療
自體HSC儲存通過采集新生兒臍帶血或成人外周血干細胞,經低溫保存后備用。其優(yōu)勢在于:
- 基因匹配無憂:自體細胞無需配型,避免異體移植的排異反應和供體短缺問題;
- 治療靈活性高:儲存的HSC可用于基因編輯(如CRISPR-Cas9修正突變基因)或直接移植,為未來療法預留空間。
公共庫建設:社會共濟的生命紐帶
截至2025年,中國造血干細胞捐獻者資料庫累計入庫超300萬人,成功配型捐獻逾2萬例。如支教女生康康的捐獻案例所示,每一份干細胞都可能成為他人重生的希望。公共庫的擴容不僅能惠及血友病患者,還可覆蓋白血病、淋巴瘤等血液疾病群體。
基因編輯技術的精準化
CRISPR-Cas9等工具的應用,使HSC的基因修飾更為高效安全。2024年,北京大學團隊利用堿基編輯技術,在患者HSC中精準修復FⅧ基因突變,動物模型中凝血功能恢復率達90%。
聯(lián)合療法的協(xié)同效應
- 干細胞+生物材料:水凝膠包裹的HSC外泌體可緩釋至關節(jié)腔,促進出血部位修復;
- 干細胞+免疫調節(jié):通過修飾HSC表達抗炎因子(如IL-10),減輕關節(jié)炎癥損傷。
政策與產業(yè)的雙重驅動
2024年,中國出臺《干細胞藥品生產許可證》制度,推動行業(yè)規(guī)范化。同時,國產重組凝血因子(如安佳因)的崛起打破外資壟斷,2023年銷售額達17.8億元,為基因治療產業(yè)化奠定基礎。
1. 個人層面:新生兒家庭可考慮臍帶血儲存,成年患者可通過動員劑采集外周血干細胞;
2. 社會層面:鼓勵更多人加入捐獻者資料庫,支持公共庫建設;
3. 專家層面:哈爾濱血液病腫瘤研究所貢鐵軍教授指出:“未來血友病治療將呈現(xiàn)‘聯(lián)合化’趨勢——基因治療糾正根本缺陷,干細胞移植重建造血系統(tǒng),輔以靶向藥物控制并發(fā)癥。”
4.政策層面:呼吁將干細胞儲存納入醫(yī)保補貼,加速基因治療審評審批。
在世界血友病日之際,讓我們以科學為炬,以愛心為帆,共同點亮血友病等疾病治愈的曙光!

 0311-86576536
0311-86576536 新聞中心
新聞中心 風采展示
風采展示 信息公告
信息公告
 公眾號
公眾號 視頻號
視頻號

